RESEARCH最新の研究内容
急性リンパ性白血病の免疫療法が更に進展! research
急性リンパ性白血病の免疫療法が更に進展!
-CAR-T細胞療法の安全性評価のための新システム開発と名大発のCAR-T細胞療法の安全性評価-
名古屋大学大学院医学系研究科(研究科長・門松 健治)小児科学の髙橋 義行(たかはし よしゆき)教授、村松 秀城(むらまつ ひでき)講師、濱田 太立(はまだ もとはる)大学院生、同医学部附属病院先端医療開発部先端医療・臨床研究支援センターの奥野 友介(おくの ゆうすけ)特任講師、西尾 信博(にしお のぶひろ)特任講師、信州大学医学部小児科学教室の中沢 洋三(なかざわようぞう)教授らの研究グループは、人工的に遺伝子を導入した細胞(以下、遺伝子改変細胞)の安全性を評価する新たな方法を開発し、これを用いて CD19 キメラ抗原受容体T細胞(Chimeric Antigen Receptor T-cell: CAR-T 細胞)の安全性を検討しました。本研究成果は、学術出版社 Cell Press と Lancetから共同発行されている科学誌「EBioMedicine」(英国時間 2018年8月3日付電子版)に掲載されました。
急性リンパ性白血病(acute lymphoblastic leukemia: ALL)に対して、人工的に遺伝子を組み込んだ(遺伝子を「導入する」)CAR-T 細胞療法の臨床応用が進み、再発・難治性の ALL に対する有効性が海外から報告されています。
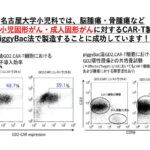
CAR-T 細胞療法は、体外で患者の T 細胞に CAR 遺伝子を導入することで、T 細胞が白血病細胞を集中的に攻撃するようにして患者の体内に戻す新規の治療方法です。海外では、レトロウイルスやレンチウイルスといったウイルスを用いた方法で CAR-T 細胞が作成されていますが、本院小児科では、製造コストや安全面を考慮してウイルスを用いず、酵素を利用したpiggyBac トランスポゾン法での CAR-T 細胞を開発しています。
一方で、遺伝子改変細胞は、遺伝子が組み込まれる場所(以下、遺伝子挿入部位)によって、時には、その細胞自体が白血病化してしまうという危険性をはらんでいます。このため、細胞の白血病化に繋がり得る場所に遺伝子が組み込まれていないか、遺伝子の挿入部位を確認して、その安全性を評価することが必要です。
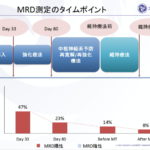
本研究グループは、CAR-T 細胞の遺伝子挿入部位を解析する新たな方法(tagmentation-assisted PCR: tag-PCR 法)を開発しました。tag-PCR 法を用いて、ウイルスを用いて作成した CAR-T 細胞と、piggyBac トランスポゾン法で作成した CAR-T 細胞の安全性を評価しました。その結果、tag-PCR 法では、既存の方法よりも短時間で正確に CAR-T 細胞の安全性を評価することができました。
また、tag-PCR 法での解析により、piggyBac トランスポゾン法で作成した CAR-T 細胞では、細胞の白血病化のリスクとなり得る場所への遺伝子挿入頻度が、ウイルスを用いて作成した CAR-T 細胞以下であることが分かりました。
本研究結果から、tag-PCR 法が遺伝子改変細胞の安全性評価において有用な方法であることが示され、今後の研究利用が期待されます。また、piggyBac トランスポゾン法で作成した CAR-T 細胞の安全性は、ウイルスを用いて作成したCAR-T 細胞と同等以上であると考えられ、今後の臨床応用が期待されます。
※ 詳細は名古屋大学のプレスリリースを御覧ください。
プレスリリースはこちら関連記事

小児がんへの理解と支援のシンボルです
皆様からいただいた寄付金は、最新の診断方法や治療を小児がんの子どもたちに届けるために使われます。世界最高レベルの医療をすべての子どもたちに届けるため、皆様のご支援ご協力をよろしくお願いいたします。
寄付する